Hierzulande gab es Befürchtungen, dass der Start desEU-weiten Fälschungsschutzsystems im Chaos enden könnte. Vereinzelt berichtenApotheker nun über Unsicherheiten. Schaut man sich in anderen Ländern Europas um, offenbaren sich aber noch viel größere Probleme: In Großbritannien ist nurdie Hälfte der Apotheken angebunden, in Frankreich streiten sich die Apotheker mitdem Gesundheitsministerium noch um die Umsetzung des Systems und Norwegenspricht von „vielen Einschränkungen“. DAZ.online hat sich in einigen Ländernumgehört. Ein Überblick.
Die EU-Fälschungsschutzrichtlinie sollte in allen 31 Staatendes Europäischen Wirtschaftsraums bis zum 9. Februar umgesetzt werden. In allenEU-Staaten plus Liechtenstein, Norwegen und Island müssen Arzneimittel also mitzusätzlichen Sicherheitsmerkmalen, einem 2D-Code und einem Erstöffnungsschutz ausgestattet sein, zudemmüssen Vorrichtungen zum Erkennen von Fälschungen getroffen werden. EineAusnahme gilt für Griechenland, Italien und Belgien – diese drei Länder habenbis 2025 Zeit bekommen, sich dem System anzuschließen, weil dort schon eigeneSicherheitssysteme installiert waren.
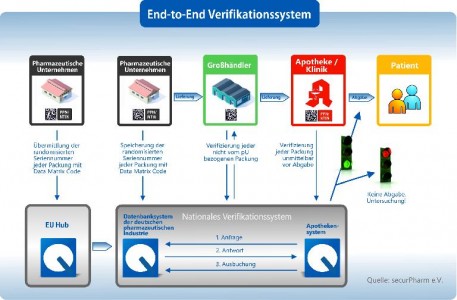
Beim neu installierten Fälschungsschutzsystem gilt in allenteilnehmenden Ländern das Ende-zu-Ende-Verifikationssystem: Das eine Ende istder Hersteller, der ein Arzneimittel mit dem 2D-Code bedruckt und in Verkehrbringt. Das andere Ende ist die Apotheke, die den Code scannt und das Präparatabgibt. Dieses Verifikationssystem funktioniert zunächst auf nationaler Ebene:Der Hersteller speichert die individuellen Packungsmerkmale in einer nationalenDatenbank. Die Apotheker scannt das Präparat, greift somit auf den Server zu undkann die Packung letztlich ausbuchen.
Nationales und europäisches Verifikationssystem
Allerdings sind die nationalen Verifikationssysteme eingebettetin ein europäisches Netzwerk, um auch grenzüberschreitend den Patientenschutzzu gewährleisten. Deswegen müssen die Hersteller die individuellen Merkmale derPackungen auch in den sogenannten EU-Hub übertragen, der von der EuropeanMedicines Verification Organisation (EMVO) betrieben wird. Der EU-Hub sorgt fürden Datenaustausch zwischen den einzelnen europäischen Ländern. Heißt konkret:Um Fälschungen auch nach einem innereuropäischen Arzneimittelhandel feststellenzu können, müssen die Länder kommunizieren. Es muss klar sein, wo welchePackung herkommt und wo sie abgegeben wurde.
Bei der Installation der nationalen Systeme gab esallerdings in einigen Ländern große Probleme in den vergangenen Monaten. Auchhierzulande war der Start holprig: Apotheker berichten von Fehlalarmen, vor demStart wurde darüber spekuliert, ob auch wirklich alle Hersteller dieindividuellen Packungsmerkmale ins Verifikationssystem übertragen können. DochRecherchen von DAZ.online zeigen, dass das Fälschungssystem in Deutschland im Vergleichzu anderen Ländern gut entwickelt ist. Hier einige Beispiele:
Quelle: Den ganzen Artikel lesen
